عنوان الموضوع : موسوعة اختبارات الفصل الثالث لا تفوتوها
مقدم من طرف منتديات العندليب
اليوم جاتني فكرة حول التحضير الجيد للفصل الثالث
هذا التحضير لازم يكون في العطلة و انا بغيت نخصص هذا الموضوع لاي شخص عنده فروض او اختبارات للفصل الثالث يحطها هنا لتسهل المراجعة
اتمنى تعجبكم الفكرة
انا غادي نبدا
اليكم بعض المواضيع في مختلف المواد
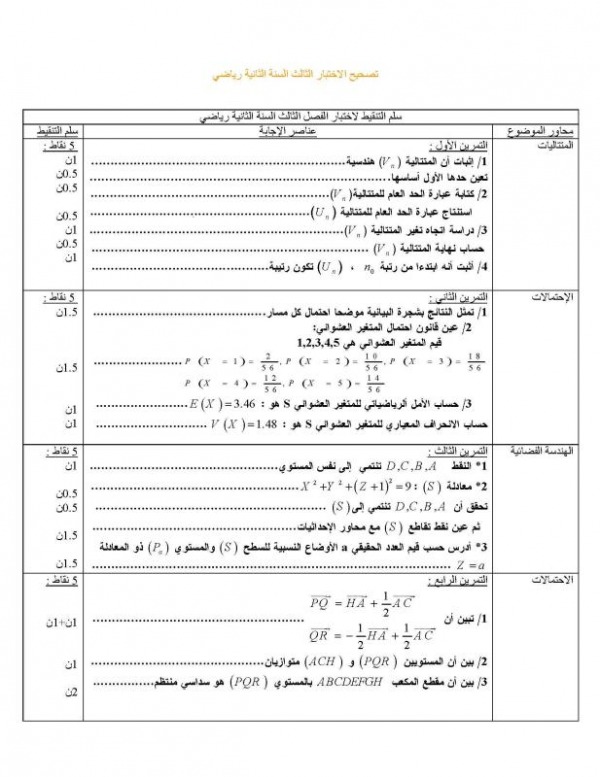
التصحيح النموذجي
هذه كلها مواضيع رياضيات ساوافيكم بنماذج المواد الاخرى لاحقا
>>>>> ردود الأعضـــــــــــــــــــاء على الموضوع <<<<<
==================================
>>>> الرد الأول :
الان مع اختبارات في الفيزياء
الجمهورية الجزائرية الديمقراطية الشعبية
المستوى: 2 ع ت , 2 ر المدة: 2سا
الفرض الثاني للثلاثي الثالث في مادة العلوم الفيزيائية
التمرين الأول:
رمز محلول ثنائي كرومات البوتاسيوم هو: (2k+ + CrO72-) يتفاعل هذا المحلول مضافا إليه حمض الكبريت مع محلول كبريتات الحديد الثنائية (Fe2+ + So42-) فتتأكسد شارذة الحديد و ترجع شارذة الكرومات (CrO72-) إلى شارذة (Cr3+).
1/ حدد الثنائية (OX/Red) الداخلتين في التفاعل.
2/ اكتب المعادلة النصفية للأكسدة و الإرجاع.
3/ اكتب المعادلة الإجمالية للأكسدة الإرجاعية.
4/ إذا علمت أن V(Fe2+ + So42-)= V1 = 25ml و أن تركيزه C1 مجهول و كان حجم (2k+ + Cr2O72-) اللازم هو V2 = 10 ml و تركيزه C2 = 0.1 mol/l
أ- شكل جدول التقدم للتفاعل الحادث.
ب- احسب تركيز محلول (Fe2+ + So42-) المستعمل ؟
5/ صف أين نقوم بوضع (Fe2+ + So42-) و (2k+ + Cr2O72-).
التمرين الثاني:
تعطى معادلات التفاعلات الكيميائية التالية:
C6H5CO2H + NH2OH → C6H5CO2-+NH3OH+
C6H8O6 + NH3 → C6H7O6- + NH4
CH3CO2H + Po43- → CH3CO2- + HPo42-
1/ هل التفاعلات الموافقة هي تفاعلات حمض- أساس ؟ لماذا ؟
2/ أعطي الثنائيتين أساس/حمض المشاركتين في التفاعل و المعادلتين حمض-أساس الموافقتين لهما.


الفرض الأول للثلاثي الثالث في العلوم الفيزيائية
المستوى: 2 ثانوي ع ت المدة: ساعة
التمرين الأول: 10 نقاط
I: نحضر محلولا بإذابة غاز النشاذر NH3 في الماء
1- اكتب معادلة التفاعل الحادث
2- ما هي الثنائيات ( أساس / حمض ) الداخلة في التفاعل مع التعليل
II: نأخذ حجما va=10ml من محلول حمض كلور الهيدروجين تركيزه المولي C= 0.01 mol/l
و نعايره بمحلول ماءات الصوديوم تركيزه المولي C= 0.1 mol/l و باستعمال كاشف ملون مناسب و هو الفينول فتالين:
1- اكتب معادلة التفاعل الكيميائي الحادث . ما نوعه ؟
2- أعطي الثنائيات ( أساس / حمض ) الداخلة في التفاعل . ماذا تلاحظ ؟ ماذا تستنتج ؟
3- ما هو الغرض من استعمال الفينول فتالين ؟ و ما هو لونه في الأوساط الحمضية و الأساسية ؟
4- ما هو حجم الأساس اللازم للحصول على التكافؤ
التمرين الثاني: 10 نقاط
I: حدد الثنائية ( مرجع / مؤكسد ) في التحولات المنمذجة بالمعادلات النصفية محددا تفاعل الأكسدة و الإرجاع بعد تعريفهما
1- Cu2+ + 2e- → Cu
2- Ag+ + 1e- → Ag
3- Mno-4 + 8H3O+ + 5e- → Mn2+ + 12H2O
4- Cr2O72- + 14 H3O+ + 6e- → 2Cr3+ + 21 H2O4
II: في كأس بيشر نضع حجما من محلول كبريتات النحاس CuSo4 تركيزه المولي 0.1mol/l . نغمس فيه صفيحة من الزنك و بعد مدة معينة نلاحظ اختفاء اللون الأزرق للمحلول في البيشر و ظهور راسب آجوري على صفيحة الزنك.
1- احسب التركيز المولي للشوارذ الموجودة في البيشر قبل وضع صفيحة الزنك.
2- فسر ماذا حدث , اكتب المعادلتين النصفيتين للأكسدة و الإرجاع.
3- اكتب المعادلة الإجمالية للتفاعل الحادث.
الفرض الأول للثلاثي الثالث في العلوم الفيزيائية
المستوى: 2 ثانوي ع ت المدة: ساعة
التمرين الأول: 10 نقاط
I: نحضر محلولا بإذابة غاز النشاذر NH3 في الماء
1- اكتب معادلة التفاعل الحادث
2- ما هي الثنائيات ( أساس / حمض ) الداخلة في التفاعل مع التعليل
II: نأخذ حجما va=10ml من محلول حمض كلور الهيدروجين تركيزه المولي C= 0.01 mol/l
و نعايره بمحلول ماءات الصوديوم تركيزه المولي C= 0.1 mol/l و باستعمال كاشف ملون مناسب و هو الفينول فتالين:
1- اكتب معادلة التفاعل الكيميائي الحادث . ما نوعه ؟
2- أعطي الثنائيات ( أساس / حمض ) الداخلة في التفاعل . ماذا تلاحظ ؟ ماذا تستنتج ؟
3- ما هو الغرض من استعمال الفينول فتالين ؟ و ما هو لونه في الأوساط الحمضية و الأساسية ؟
4- ما هو حجم الأساس اللازم للحصول على التكافؤ
التمرين الثاني: 10 نقاط
I: حدد الثنائية ( مرجع / مؤكسد ) في التحولات المنمذجة بالمعادلات النصفية محددا تفاعل الأكسدة و الإرجاع بعد تعريفهما
1- Cu2+ + 2e- → Cu
2- Ag+ + 1e- → Ag
3- Mno-4 + 8H3O+ + 5e- → Mn2+ + 12H2O
4- Cr2O72- + 14 H3O+ + 6e- → 2Cr3+ + 21 H2O4
II: في كأس بيشر نضع حجما من محلول كبريتات النحاس CuSo4 تركيزه المولي 0.1mol/l . نغمس فيه صفيحة من الزنك و بعد مدة معينة نلاحظ اختفاء اللون الأزرق للمحلول في البيشر و ظهور راسب آجوري على صفيحة الزنك.
1- احسب التركيز المولي للشوارذ الموجودة في البيشر قبل وضع صفيحة الزنك.
2- فسر ماذا حدث , اكتب المعادلتين النصفيتين للأكسدة و الإرجاع.
3- اكتب المعادلة الإجمالية للتفاعل الحادث.
التمرين الأول05نقاط)
1- أجب بصح أو خطأ مع تصحيح الخطأ إن وجد:
أ-قيمة الحقل المغناطيسي لقضيب مغناطيسي تتغير من نقطة لأخري
ب-يحدد الوجه الجنوبي للوشيعة يجتازها تيار ثابت الشدة . اعتمادا علي قاعدة دوران عقارب الساعة . بحيث يكون وجهها الجنوبي يوافق دوران التيار عكس عقارب الساعة لمراقب ينظر اليها .
جـ- المكثفة تلعب دور قاطعة في التيار المستمر عندما تشحن .
د-يمكن تجسيد الطيف المغناطيسي ببرادة الألمنيوم .
هـ- في وشيعة طويلة يجتازها تيار ثابت تدخل خطوط الحقل المغناطيسي من الوجه الشمالي وتخرج من الوجه الجنوبي .
تمرين (2):
في الشكل المقابل عند غلق القاطعة ينجذب الضيب المغناطيسي الي الوشيعة .
1)- حدد وجهي الوشيعة
2)- حدد قطبي المغناطيس
تمرين(3):
نربط مكثفة مشحونة على التسلسل مع مقاومة Ω R=1K ونغلق القاطعة
1- عند 0 = tتعطى تغيرات التوتر بين طرفي المكثفة بالعلاقة حيث uc(v)و t(s).
1- مثل برسم الدارة السابقة مع تحديد اتجاه التيار و تمثيل uC و uR بأسهم في الدارة .
2- أوجد المعادلة التفاضلية للدارة وبين أنها تقبل كحل لها عبارة .
3- بين صحة أو خطأ ما يلي
أ- ثابت الزمن للدارة ( RC ) هو s =1
ب- تفرغ المكثفة بنسبة %99 بعد زمن قدرة =5 ms
د- سعة المكثفة هي F C=1 .
ه – استنتج عبارة (i(t ثم مثلها كيفيا مع حساب قيمة I0 حيث 5V E= .
و- وضح علي هذا الرسم طريقة حساب ثابت الزمن ( ) بيانيا.




الاختبار الأخير في مادة العلوم الفيزيائية
التمرين الأول ( 8 نقاط) :
1- لمعرفة بنية حمض الميثانويك ( حمض النمل ) والذي صيغته الجزيئية HCOOH، نضع كمية منه في وعاء تحليل كهربائي موصول مع مولد في دارة على التسلسل .
نغلق القاطعة فنلاحظ عدم مرور تيار كهربائي .
- ماذا تستنتج فيما يخص بنية حمض الميثانويك النقي؟ ( 0.5 )
2- نقوم الأن بإذابة كتلة m من حمض الميثانويك في لتر من الماء المقطر فنحصل على محلول شاردي نسميه (Sa)تركيزه Ca .
- ماهو الأساس المرافق لحمض الميثانويك ؟ أكتب الثنائية أساس/حمض الموافقة .( 0.5ن + 0.5ن )
3- نأخذ حجم Va= 20mLمن المحلول) (Sa ونضيف له قطرتين من أزرق البروموتيمول ثم نعايره بمحلول الصود (Na+(aq)+HO-(aq)) تركيزه Cb= 0.2mol.L-1 فنلاحظ تغير اللون بعد سكب حجم Vb=10ml من الصود .
- اذكر اللون الذي يأخذه الكاشف الملون عند بداية المعايرة ،عند نقطة التكافؤ وبعدها ؟ ( 0.75ن )
4- يعطى لك التجهيز المستعمل في عملية المعايرة .
- سم البيانات المرقمة؟ ( 1.5ن )
- أكتب معادلة تفاعل المعايرة الحاصل في الزجاجية 4؟ ( 1ن )
- أحسب التركيز المولي للمحلول الحمضي ثم إستنتج قيمة الكتلة m المستعملة؟ ( 1.25ن + 0.5ن )
5- نأخذ حجم من المحلول (Sa) و نمدده 50 مرة فنحصل على محلول ممدد نسميه (S) :
أ- احسب التركيز الموليC للمحلول) (S . ( 0.5ن )
ب- احسب الناقلية النوعية σ للمحلول) (S عند25°C علما أن الناقلية النوعية المولية للشوارد المتواجدة في المحلول عند هذه الدرجة هي :
35 mS.m2.mol-1 = H3O+λ mS.m2.mol-1 = 5,46 HCOO- λ
وباعتبار تفكك الحمض في الماء كلي . ( 1ن )
يعطى: = 46 g.mol-1 M HCOOH
1
التمرين الثاني : ( 7نقاط )
نمزج Lm100 من محلول مائي لبرمنغنات البوتاسيوم 4OnMK تركيزه المولي 1- L.lom0.02 مع
Lm100 من محلول مائي لحمض الأوكساليك euqilaxo edica 4O2C2H تركيزه المولي
1- L.lom0.02 في وسط حمضي .
يحدث تفاعل كلي معادلته الحصيلة :
2MnO4- + 5H2C2O4 + 6H+ 2Mn2+ + 10CO2 + 8H2O
1- عرف المؤكسد والمرجع . ( 0.5ن )
2- تعطى لك الثنائيتين مرجع / مؤكسد الداخلتين في التفاعل :
MnO4- / Mn2+ و CO2 / H2C2O4
- أكتب المعادلتين النصفيتين الإلكترونيتين الموافقتين . ( 1ن )
- ما هو دور الوسط الحمضي الذي تم فيه التفاعل ؟ ( 0.5ن )
3- أحسب كمية مادة حمض الأوكساليك وكمية مادة شوارد البرمنغنات الإبتدائيتين . ( 1ن )
4- أنشيء جدول تقدم التفاعل . ( 2ن )
5- تعطى لك 4 إقتراحات ، ما هو الإقتراح أو الإقتراحات الصحيحة :
* كل جزيئات حمض الأوكساليك اختفت و تبقت شوارد البرمنغنات .
* لا يحتوي المحلول المزيج عل جزيئات الحمض ولا على شوارد البرمنغنات .
* تبقى lomm1.2 من شوارد البرمنغنات .
* تشكل lomm0.4 من شوارد المنغنيز . ( 2ن )
التمرين الثالث : ( 5نقاط )
1- تعطى لك الكتابات التالية لمركب عضوي ، أعط تسمية كل منها .
.......................... ...................... .......................... .........................
.......................... ...................... .......................... .........................
2- مُثلت ثلاث مركبات عضوية بإحدى الكتابات السابقة ، أعط الصيغة المجملة لكل مركب .
3- أذكر العائلة الكيميائية التي ينتمي إليها كل مركب .
الصيغ المجملة : ( A ) ..................... ( B ) ........................... ( D ) .........................
العائلة الكيميائية : ( A ) ......................... ( B ) ......................... ( D ) .......................
4- سم المركبات التالية و أعط صيغة المجموعة الوظيفية لكل مركب .
.................................................. ......... .................................................. ........
....................... .......................
.................................................. ....... .................................................. ........
........................ .......................
CH3 – CH – CH – COOH .................................................. .........
׀ ׀ .......................
CH3 CH3 ( 0.25 نقطة لكل جواب )


الجمهورية الجزائرية الديمقراطية الشعبية
المستوى: 2 ع ت , 2 ر المدة: 2سا
الفرض الثاني للثلاثي الثالث في مادة العلوم الفيزيائية
التمرين الأول:
رمز محلول ثنائي كرومات البوتاسيوم هو: (2k+ + CrO72-) يتفاعل هذا المحلول مضافا إليه حمض الكبريت مع محلول كبريتات الحديد الثنائية (Fe2+ + So42-) فتتأكسد شارذة الحديد و ترجع شارذة الكرومات (CrO72-) إلى شارذة (Cr3+).
1/ حدد الثنائية (OX/Red) الداخلتين في التفاعل.
2/ اكتب المعادلة النصفية للأكسدة و الإرجاع.
3/ اكتب المعادلة الإجمالية للأكسدة الإرجاعية.
4/ إذا علمت أن V(Fe2+ + So42-)= V1 = 25ml و أن تركيزه C1 مجهول و كان حجم (2k+ + Cr2O72-) اللازم هو V2 = 10 ml و تركيزه C2 = 0.1 mol/l
أ- شكل جدول التقدم للتفاعل الحادث.
ب- احسب تركيز محلول (Fe2+ + So42-) المستعمل ؟
5/ صف أين نقوم بوضع (Fe2+ + So42-) و (2k+ + Cr2O72-).
التمرين الثاني:
تعطى معادلات التفاعلات الكيميائية التالية:
C6H5CO2H + NH2OH → C6H5CO2-+NH3OH+
C6H8O6 + NH3 → C6H7O6- + NH4
CH3CO2H + Po43- → CH3CO2- + HPo42-
1/ هل التفاعلات الموافقة هي تفاعلات حمض- أساس ؟ لماذا ؟
2/ أعطي الثنائيتين أساس/حمض المشاركتين في التفاعل و المعادلتين حمض-أساس الموافقتين لهما.
تمرين (1):
1. كيف يهتدي الربان في البحر؟
2. كيف يجسد الطيف المغناطيسي لقضيب مغناطيسي ؟
3. هل يوجد فرق بين الطيفين المغناطسين لكل من قضيب مغناطيسي ووشيعة طويلة يجتازها تيار كهربائي ثابت؟
4. أجب بصح أو خطأ مع تصحيح العبارة الخاطئة إن وجدت .
أ- الوشيعة تتميز بوجهين ثابتين بغض النظر عن جهة التيار الكهربائي .
ب- في تجربة لا بلاص اذا كان شعاع الحقل المغناطيسي B موازيا للناقل فإن القوة التي يخضع لها الناقل غير معدومة ( F≠0 )
تمرين (2):
في الشكل المقابل يمر تيار(I )عبر ناقل طويل و ينتج
في النقطة (a )حقلا مغناطسيا B
1-حدد اتجاه التيار .
2 -حدد اتجاه الحقل المغناطيسي B2 الناتج
في النقطة (b (حيث R1.R2 بعد الحقل B عن الناقل .
تمرين (3):
نشحن مكثفة سعتها C = 5µF تحت توتر E = 6V ثم نفرغها بناقل أو مي 1KΩ =R .
1. أنجز رسما تخطيطيا للدرة التفريغ بإسخدام الرموز النظامية مع تحديد إتجاه التيار وتمثيل كل UR و Uc بـأسهم .
2. بين صحة أو خطأ ما يلي مع التبرير.
.
في حالة التفريغ يكون
1-عند 0 = t.
أ- Uc(0) = 0
ب- قيمة ثابت الزمن 5ms= .
جـ -عند يكون , لما .
د- مثل كيفيا تغيرات Uc=ƒ(t) مع توضيح طريقة تعيين( ) بيانيا علي هذا البيان .



الاختبار الأخير في العلوم الفيزيائية
ثانية ثانوي علوم تجريبية
ــــــــــــــــــــــــــــــــــــــــــــــــــ ــــــــــــــــــــــــــــــــــــــــــــــــــ ــــــــــــــــــــــــــــــــــــــــــــــــــ ـــــــــــــــــــــــــــ
التمرين الأول:
نعطي معادلات التفاعلات التالية :
1/ هـل هذه التفاعلات تفاعلات حمض-أساس ؟ علل إجابتك؟
2/تعرف في كل حالة على الحمض و الأساس
3/أعط الثنائية أساس/حمض المشاركة في كل تفاعل وأكتب المعادلات النصفية لها ؟
التمرين الثاني:
أستر(E) صيغته المجملة C5H10O2 تحصلنا عليه من تفاعل حمض كاربوكسيلي (A) صيغته H-COOH (حمض النمل) مع مركب (C) صيغته R-OH
أ- ماهي طبيعة المركب (C) .
ب - أكنب الصيغة المجملة للمركب (C) ثم أكتب الصيغ نصف المفصلة الممكنة لهذا المركب (C) مع التسمية .
جـ- أكتب معادلة التفاعل الكيميائي الحادث بإستعمال الصيغ المجملة .
ب- إن تفاعل 9.2 g من الحمض (A) مع 14.8 g من المركب (C) وعند بلوغ التفاعل حده نتحصل على كتلة قدرها
12.24 g من الأستر (E) .
1 - أحسب عدد مولات كل من المركبين (A) ، (C) ثم أستنتج أن المزيج متساوي المولات .
2 - أحسب عدد مولات الأستر (E) ثم إستنتج مردود التقاعل .
3 - حدد صيغة المركب المستخدم (C) من بين الصيغ المفصلة السابقة ،
C =12g/mol ، H =1 g/mol ، O =16g/mol
التمرين الثالث:
ناقلان مستقيمان ومتوازيان وأفقيان البعد بينهما d = 5 cm نربط طرف كل ناقل بمولد كهربائي .
يمكن لقضيب AC أن ينتقل على الناقلين (كما في الشكل) .
عند تشغيل المولد يمر في القضيب تيار شدته I = 6 A جهته من A إلى C
نضع المجموعة في حقل كهربائي منتظم شدته B = 0.2 T
1- إستنتج حامل وجهة القوة الكهرومغناطسية في الحالتين التاليتين :
أ / عمودي على مستوي الناقلين ومتجه نحو الأعلى .
ب / في مستوي الناقلين ويوازيهما .
2 – أحسب شدة القوة الكهرو مغناطسية في حالة عمودي على مستوي الناقلين ومتجه نحو الأعلى .
3 – نربط في منتصف القضيب AC خيط مهمل الكتلة وعديم الإمتطاط يمر على محز بكرة خفيفة ، وفي طرفه
الثاني نعلق جسم كتلته M = 10 g
أ - عيّن خصائص القوة المطبقة في منتصف القضيب من طرف الخيط على القضيب . هل يتوازن القضيب ؟ .
ب – يرتفع الجسم بـ 20cm .
– أحسب عمل ثقل الجسم خلال الصعود . أحسب عمل قوة لابلاس خلال الحركة .
ــــــــــــــــــــــــــــــــــــــــــــــــــ ــــــــــــــــــــــــــــــــــــــــــــــــــ ــــــــــــــــــــــــــــــــــــــــــــــــــ ـــــــــــــــــــــــــــ


الجمهورية الجزائرية الديمقراطية الشعبية
المستوى: 2 ع ت , 2 ر المدة: 2سا
الفرض الثاني للثلاثي الثالث في مادة العلوم الفيزيائية
التمرين الأول:
رمز محلول ثنائي كرومات البوتاسيوم هو: (2k+ + CrO72-) يتفاعل هذا المحلول مضافا إليه حمض الكبريت مع محلول كبريتات الحديد الثنائية (Fe2+ + So42-) فتتأكسد شارذة الحديد و ترجع شارذة الكرومات (CrO72-) إلى شارذة (Cr3+).
1/ حدد الثنائية (OX/Red) الداخلتين في التفاعل.
2/ اكتب المعادلة النصفية للأكسدة و الإرجاع.
3/ اكتب المعادلة الإجمالية للأكسدة الإرجاعية.
4/ إذا علمت أن V(Fe2+ + So42-)= V1 = 25ml و أن تركيزه C1 مجهول و كان حجم (2k+ + Cr2O72-) اللازم هو V2 = 10 ml و تركيزه C2 = 0.1 mol/l
أ- شكل جدول التقدم للتفاعل الحادث.
ب- احسب تركيز محلول (Fe2+ + So42-) المستعمل ؟
5/ صف أين نقوم بوضع (Fe2+ + So42-) و (2k+ + Cr2O72-).
التمرين الثاني:
تعطى معادلات التفاعلات الكيميائية التالية:
C6H5CO2H + NH2OH → C6H5CO2-+NH3OH+
C6H8O6 + NH3 → C6H7O6- + NH4
CH3CO2H + Po43- → CH3CO2- + HPo42-
1/ هل التفاعلات الموافقة هي تفاعلات حمض- أساس ؟ لماذا ؟
2/ أعطي الثنائيتين أساس/حمض المشاركتين في التفاعل و المعادلتين حمض-أساس الموافقتين لهما.


انتظروا مواضيعي الاخرى و شكرا


=========
>>>> الرد الثاني :
واو رائع انت طالبة في 2 ثانوي رياضي هدا حلمي انا طالبة 1 ثانوي علمي اتمنى ان نبقى على تواصل لاطرح عليك اسئلتي ان كان هدا لا يزعجك طبعااااا شكراااا
=========
>>>> الرد الثالث :
المشاركة الأصلية كتبت بواسطة fifi tery 
واو رائع انت طالبة في 2 ثانوي رياضي هدا حلمي انا طالبة 1 ثانوي علمي اتمنى ان نبقى على تواصل لاطرح عليك اسئلتي ان كان هدا لا يزعجك طبعااااا شكراااا
مرحبا فيفي
حلمك ليس بمستحيل تقدري تحقيه بسهولة
اما بالنسبة لاستفساراتك فهي غير مزعجة على الاطلاق
بالعكس انا نحب نساعدك
و اذا درتي شعبة رياضيات مثلي
غادي نبعثلك مواضيعي في كل المواد

=========
>>>> الرد الرابع :
بتوفيق لكم جميعا
=========
>>>> الرد الخامس :
شكرا لك
و بالتوفيق للجميع
=========
merci c génial
de rieeeeeeeeeeeeen
جزاك الله كل خير على مجهوداتك

merciiiiiiiiiiiiiiiiiiiiiiiiii
[COLOR="DarkOrchid"] شكرا لك /COLOR]
شكرا لك جزاك الله خيرا يعطيك العافية

waaaaaaaaaaaaaaaaaaaaaaaaaaaaaaw chokraaaaaaaaaaaan liiiiiiiiiiiiiiiiiiik habobaaaaaati alah ywafkak f kol haja f hyaak chokran lik
المشاركة الأصلية كتبت بواسطة foufou 95 
waaaaaaaaaaaaaaaaaaaaaaaaaaaaaaw chokraaaaaaaaaaaan liiiiiiiiiiiiiiiiiiik habobaaaaaati alah ywafkak f kol haja f hyaak chokran lik
merci hbiba raby ykhlik


































 رد مع اقتباس
رد مع اقتباس